巨噬细胞是是一种广泛分布于全身的免疫细胞,在先天性免疫和获得性免疫反应中都起着重要作用。其中,吞噬作用是指巨噬细胞识别并吞噬病原体或其他异物(包括肿瘤细胞以及自身衰老和异常的红细胞等)的过程,涉及细胞形态改变、骨架重构、表面粘附、细胞突出和信号转导等复杂的协同行为。这一过程引起了生物物理和生物力学领域的广泛关注。长期以来,研究人员致力于发展理论模型来解析在此过程中巨噬细胞如何有效变形并完成吞噬,但现有模型往往无法考虑细胞骨架重构和细胞膜-细胞骨架相互作用,导致模型分析与实验数据出现较大差异。为此,从巨噬细胞结构出发构建包含细胞膜和细胞骨架信息的细胞力学模型,可为从分子到细胞等不同层面探究吞噬过程中细胞膜和细胞骨架的动力学行为提供新途径。
近日,浙江大学李学进研究员课题组在Cell Press旗下期刊Biophysical Journal上发表题为“Two-component macrophage model for active phagocytosis with pseudopod formation”的封面论文。该研究构建了一种新型的双组分巨噬细胞力学模型,通过设计细胞骨架生长、回缩、断裂和重构等功能以及膜面积补充算法,成功再现了巨噬细胞吞噬病原体或其他异物过程中吞噬行为的模拟(图1),揭示了细胞骨架变化和伪足形成在调控吞噬行为中的关键作用。
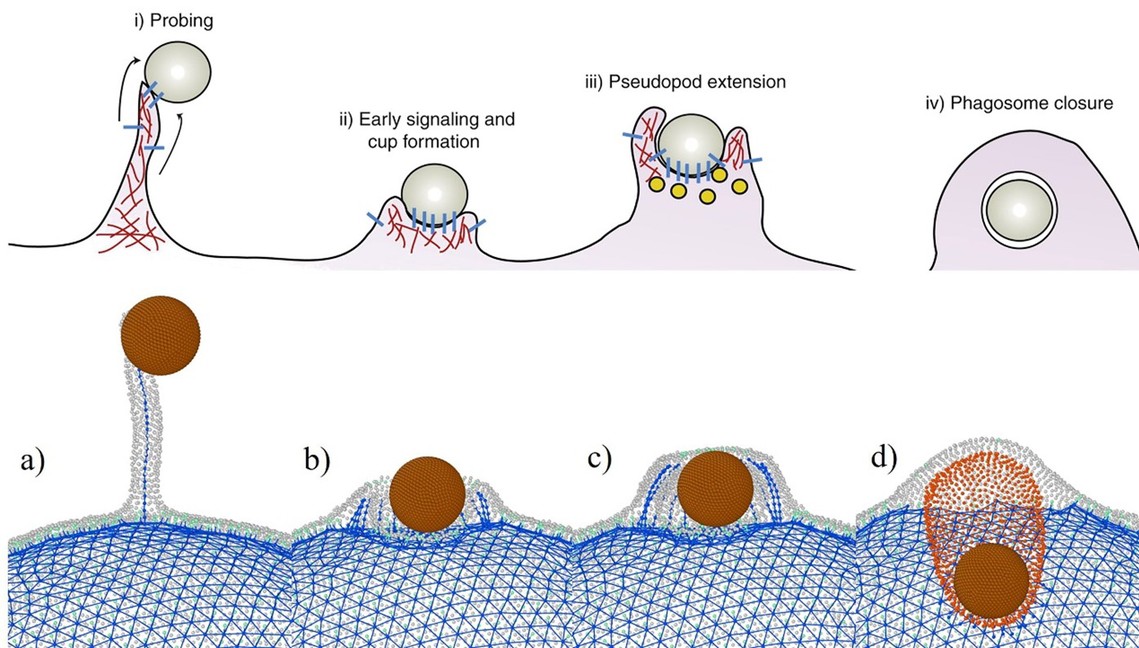
图1 巨噬细胞通过伸出伪足主动吞噬目标物的过程。
文章发表后,美国生物物理学会在官方博客以“Macrophages detect and engulf targets with pseudopods”为题进行了推介;同时,Biophysical Journal期刊在当期的News and Notable栏目中以“Particle-based simulations shed light on cytoskeleton-membrane dynamics in phagocytosis”为题进行了亮点报道,认为该方法能够把细胞膜的微观结构变化(微观尺度)与细胞伪足形成引起的吞噬行为(介观尺度)联系起来,为理解吞噬过程中巨噬细胞膜和细胞骨架动力学交互行为提供了一个模型框架。同时,该研究证实了细胞突出是形成伪足结构的主要驱动力,为探究吞噬过程驱动作用的不确定性提供了新观点。这些发现对于在不同情形下控制巨噬细胞吞噬率有重要指导意义,从诱导巨噬细胞吞噬癌细胞以抑制肿瘤细胞生长,到规避巨噬细胞吞噬递药微粒以增强靶向递药效率等方面。

